obiecte
- Transplant de măduvă osoasă
- Semnalizare celulară
- chimioterapie
- mielom
În ciuda progreselor terapeutice majore recente în mielomul multiplu, regresia/progresia bolilor refractare, în special după auto-SCT, rămâne o provocare nesatisfăcută în domeniu. Din punct de vedere genetic, s-a raportat o mutație frecventă a RAS la mielom. 1 În plus, pacienții cu mutație NRAS au fost asociați cu susceptibilitate redusă la bortezomib. 2 Prin urmare, este vizată terapia de activare anti-RAS. Sorafenib este un inhibitor multi-kinază care vizează activarea RAS. Pe de altă parte, sa demonstrat că bortezomibul restabilește chemosensibilitatea la alchilatori din mielomul refractar. 4 Această lucrare prezintă pacienții cu mielom refractar bortezomib și lenalidomidă cu activare ERK1/2 datorită mutației V600E BRAF, care a dus la sorafenib într-un răspuns susținut, dar combinația ulterioară de bortezomib/bendamustină/dexametazonă (VBD) a furnizat PR.
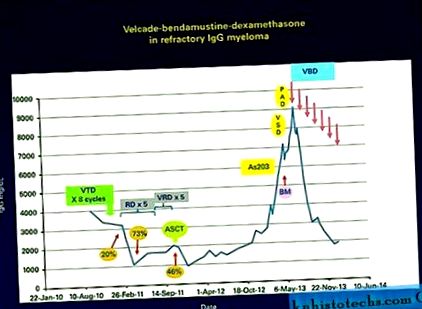
Tratamentul și răspunsul IgG seric pe parcursul evoluției bolii. Pacientul a obținut doar un răspuns de paraproteină de 20% după opt cicluri de VTD și PR tranzitoriu, dar persistent pe RD, care în cele din urmă a fost rezistent la VRD. PR-ul foarte bun a fost realizat cu auto-SCT, dar boala a progresat 9 luni mai târziu, în care As203/dex a început fără răspuns. A fost efectuată aspirația BM, care a dezvăluit activarea ERK constitutivă și, prin urmare, a fost inițiată pe VSD cu un răspuns minor nedeterminat. Boala a continuat în ciuda salvării PAD, dar a ajuns la PR până la VBD.
Imagine la dimensiune completă
Cariotipul pacientului, mutația RAS/RAF, metilarea RASSF1A și activarea ERK1/2. FISH pentru amp (1q21), del (17p), t (4; 14) și t (14; 16) au arătat doar prezența amperului (1q21). Secvențierea NRAS, KRAS și BRAF a arătat o mutație V600E BRAF. PCR specifică metilării a indicat nemetilarea promotorului RASSF1A (UU). Analiza Western blot a celulelor plasmatice BM sortate CD138 a arătat activarea ERK1/2. ++, fosfo-ERK1/2 pozitiv; UU, nemetilare; WT, tip sălbatic. Celulele HeLa și KMS-12-BM au servit drept controale pozitive și negative pentru activarea ERK.
Imagine la dimensiune completă
Sa demonstrat că acest pacient este rezistent la bortezomib și lenalidomidă chiar și în timpul inducției. În ciuda obținerii unui PR foarte bun după auto-SCT, boala sa a progresat la 9 luni după auto-SCT, indicând mielom foarte refractar, dovadă fiind progresia bolii agresive cu niveluri de IgG în creștere rapidă. În plus, pe măsură ce boala sa a progresat în decurs de 9 luni de la auto-SCT, celulele mielomului au fost probabil chemorefractive în plus față de bortezomib, talidomidă și lenalidomidă pentru doze mari de melfalan. Din păcate, carfilzomib și pomalidomida nu erau disponibile. Prin urmare, noi terapii în loc de chimioterapie convențională au fost luate în considerare pentru recidivă.
Bendamustina este un hibrid chimic de muștar de azot și benzimidazol și, prin urmare, are proprietățile unui analog alchilant și al unui purin. Bendamustina nu este rezistentă la alte chimioterapii și este eficientă în limfomul indolent non-Hodgkin, LLC și mielom. 12 Am arătat anterior că bortezomibul poate restabili chimiosensibilitatea la pacienții cu mielom refractar la chimioterapie multiplă 4, prin urmare, au utilizat VBD cu recidivă progresivă rapidă în terapia bazată pe bortezomib la acest pacient. În concordanță cu rezistența sa încrucișată la alți agenți alchilanți, această combinație PR a realizat bendamustină. Studiile recente ale bendamustinei/prednisolonului în recidivarea/mielomul refractar au arătat într-adevăr o rată de răspuns modestă 13, dar se obține o rată de răspuns mult mai mare (60%) cu combinația de bortezomib cu bendamustină și dexametazonă. 14 În cele din urmă, rațiunea utilizării bortezomibului la pacienții refractari la bortezomib se bazează pe date in vitro și in vivo care demonstrează restabilirea chimiosensibilității agenților alchilanți în celulele mielom chemoresistente. 4
Activarea verificată funcțional a semnalizării RAS-RAF-MEK-ERK poate fi asociată cu mutația BRAF V600E în loc de mutația KRAS/NRAS sau hipermetilarea RASSF1A. Sorafenib nu este suficient de puternic pentru a obține un răspuns semnificativ în acest caz de activare RAS din cauza unei mutații BRAF și, prin urmare, necesită o încercare de vemurafenib. VBD este un regim activ chiar și la pacienții cu mielom care sunt rezistenți la regimurile pe bază de bortezomib sau de lenalidomidă, altele decât doze mari de melfalan.
consimţământ
Consimțământul informat scris a fost obținut de la pacient pentru a publica acest raport. O copie a consimțământului scris este disponibilă pentru examinare de către redactorul-șef al acestei reviste.
- Ceai de fructe pentru copii cu miere pentru un somn bun, 20x2 g Ceaiuri medicinale
- Dexametazona și riscul supresiei suprarenalei în leucemia cu mielom multiplu
- Bortezomib STADA 2,5 mgml
- Doriți o prezentare generală bună Încercați aceste 7 opțiuni
- Vreau să economisesc 50 sau 100 de euro pe lună Trebuie să iau o ofertă de la bancă sau nu este o idee bună;