obiecte
abstract
Cinci până la 10% dintre copiii cu LMA de novo și până la 23% dintre pacienții cu LMA recidivantă au o boală refractară definită ca eșec în atingerea remisiunii morfologice după două cicluri de chimioterapie. 1, 2, 3, 4 Deoarece incidența LMA la populația pediatrică din Marea Britanie este de 70 de cazuri pe an, se așteaptă ca 8-12 copii pe an să fie LMA refractară în țară. Din punct de vedere istoric, prognosticul pentru acest subgrup de pacienți a fost neutru, studii recente de cooperare sugerând supraviețuirea globală (OS) de 22 și 14% pentru LMA pediatrică refractară primară și refractară. 3, 4
Cel mai bun tratament pentru acești pacienți nu a fost încă identificat. Transplantul de celule stem hematopoietice alogene (SCT) este standardul de îngrijire pentru LMA frontală sau recidivantă cu risc crescut. 5, 6, 7 Cu toate acestea, datele privind rezultatele pacienților supuși SCT pentru boala refractară sunt înclinate. Abordări diferite și cohorte incoerente au produs rezultate foarte diferite, cu rate de supraviețuire de 0-35% și mortalitate legată de transplant (TRM) de până la 40%. 4, 9, 8, 9, 10, 11, 12, 13, 14
Mai exact, pentru copiii care nu sunt în remisiune la transplant, au fost raportați un total de 160 de pacienți în patru documente diferite. 4, 8, 10, 14 Trei dintre aceste documente (inclusiv două studii naționale prospective) documentează 0% SO pe termen lung pentru copiii cu boală activă în SCT. 4, 10, 14 În schimb, Bunin și colab. 8 s-a documentat supraviețuirea fără leucemie (LFS) de 12% la copiii cu LMA refractară primară și de 20% la pacienții refractari recurenți. În plus, 19% din SO au fost raportate într-o analiză de registru care combină datele CIBMTR pentru adulți și copii la 1428 de pacienți cu LMA în remisiune la transplant. În acest context, procentul de explozii în transplant, un donator nepotrivit sau neînrudit, starea de performanță slabă și citogenetica cu risc scăzut au fost sugerate ca posibili factori de risc combinați pentru un rezultat mai slab.
Datorită prognosticului nefavorabil al LMA refractare, o analiză recentă descurajează furnizarea de SCT la adulți cu un procent de explozii> 25% în măduva osoasă (BM) la transplant. Recomandările pentru tratamentul copiilor cu o situație similară nu sunt disponibile. Pentru majoritatea acestor pacienți, nu sunt necesare alte opțiuni de tratament alternative, astfel încât sunt necesare date suplimentare pentru a lua o decizie informată și adaptată pacientului. Acest studiu retrospectiv multicentric și-a propus să evalueze rezultatele și să identifice factorii predictivi pentru copiii care au primit primul SCT pentru LMA refractară primară sau LMA refractară recurentă cu boală activă în SCT.
Materiale și metode
pacienți
Pacienții cu vârsta cuprinsă între 0-18 ani care au suferit primul SCT alogen pentru LMA refractară primară sau recidivantă recidivantă la 1 din 13 centre de transplant pediatric din Regatul Unit între 2000 și 2012 și au fost raportați la Societatea Britanică pentru Transplant de Sânge și Transplant de Măduvă Osoasă ( BSBMT). pentru acest studiu dacă au avut o boală activă documentată în termen de 2 săptămâni de la începerea regimului de condiționare. Pacienții cu AML FAB M3 și leucemie juvenilă din mielomonocite au fost excluși din studiu. Boala refractară a fost definită ca> 5% explozii în BM fie morfologic, fie prin citogenetică sau metode moleculare sau boală extramedulară (EM) dovedită după
2 cicluri de chimioterapie de inducție/reinducție.
Eșecul primar de inducție a fost definit ca> 5% explozii în BM fie morfologic, fie prin citogenetică sau prin metode moleculare la sfârșitul celui de-al doilea ciclu de inducție.
CR a fost definit de BM cu hematopoieză normală și morfologic 6, 16
Datele sursă au fost validate pentru a confirma diagnosticul bolii refractare la toți pacienții prin examinarea morfologiei și a rezultatelor citogenetice/moleculare la momente semnificative de timp, dar nu a fost efectuată nicio analiză morfologică centralizată a aspiratului de măduvă osoasă înainte de SCT.
Consimțământul pentru datele care trebuie înregistrate în registrul BSBMT pentru analiza rezultatelor și cercetarea a fost obținut la momentul transplantului în conformitate cu liniile directoare EBMT.
Transplant
Compatibilitatea HLA cu un donator legat de adulți sau fără legătură a fost definită prin tastarea cu rezoluție înaltă/medie pentru locurile HLA-A, -B, -C, -DR, -DQ. Compatibilitatea HLA cu cablul fără legătură a fost definită ca tastarea cu rezoluție înaltă/medie pentru locurile HLA-A, -B, -DR. Compatibilitatea HLA cu un donator frate a fost definită prin tastarea cu rezoluție scăzută pentru HLA-A, -B, -C, -DR, -DQ. Donatorii au fost definiți ca frați identici HLA dacă au moștenit aceleași haplotipuri parentale ca beneficiarii lor. Perechile donator-beneficiar au fost definite ca potrivire HLA (MD) dacă erau 10/10 (donator adult) sau 6/6 (cablu) și nepotrivire HLA (MMD) altfel.
Regimurile de condiționare au fost definite ca „intensitate redusă” în conformitate cu criteriile Champlin și mieloablativ altfel. Pe scurt, un regim de condiționare a fost considerat mieloablativ dacă a provocat citopenie ireversibilă fără salvarea celulelor stem și la intensitate redusă, ducând la mielosupresie reversibilă asociată cu niveluri scăzute de toxicitate non-hematologică. 17
Obiective de studiu
Obiectivul principal al studiului a fost LFS la 5 ani după SCT la copiii cu LMA refractară primară sau recurentă recurentă transplantată în remisie. LFS a fost definit ca timpul de la transplant la recidivă sau deces din orice cauză, oricare dintre acestea apare mai întâi. Obiectivele secundare au inclus incidența GVHD acut și cronic, ratele de recidivă, TRM și 5 ani de OS. TRM a fost definit ca orice deces survenit în Republica Cehă; OS a fost definit ca timpul de la SCT până la deces, indiferent de cauză.
analize statistice
Datele pacienților au fost colectate prin baza de date BSBMT și verificate cu fiecare centru. Datele au fost verificate pentru consistență și analiza finală a fost efectuată utilizând software-ul statistic Stata (StataCorp. 2015. Stata Statistical Software: Release 14, College Station, TX: StataCorp LP) și R. Actualizarea ulterioară a fost actualizată la 1 ianuarie 2016 Rezultatele analizelor descriptive sunt date ca mediane și intervale. Estimările Kaplan-Meier și intervalele de încredere au fost utilizate pentru a estima LFS și OS, iar testul de log log (variabile discrete) și regresia Cox au fost utilizate pentru comparație. 18 pacienți au fost cenzurați la ultima urmărire dacă nu au avut loc evenimente. Incidența cumulativă a recidivelor și a TRM a fost estimată, permițând riscuri competitive folosind metoda Fine-Grey. 19 modele de regresie proporțională Prox ale riscului Cox au fost utilizate pentru a evalua efectul următoarelor variabile asupra vârstei de recidivă, LFS și OS: vârstă, grup de risc citogenetic, refractar primar versus recurent, procent de explozii în BM în SCT, regim de condiționare, tip de donator (utilizare versus nepotrivire).), utilizarea epuizării celulelor T, sursa celulelor stem și prezența GVHD acută și cronică. Intervalele de încredere sunt raportate la 95%, iar testele statistice au fost efectuate la 0,05, (bilateral).
Rezultatul
Caracteristicile pacienților
Șaizeci și unu de pacienți au fost identificați prin registrul BSBMT ca beneficiari de SCT pentru LMA refractară, nu în Republica Cehă în SCT între 2000 și 2012. Doi pacienți au fost excluși pe baza diagnosticului de leucemie mielomonocitară juvenilă și 15 pacienți au fost excluși ca validare a datelor. nu confirmă diagnosticul de LMA refractară. Au fost analizați restul de 44 de pacienți pentru care verificarea datelor sursă a confirmat boala refractară. Caracteristicile celor 44 de pacienți care au intrat în studiu sunt rezumate în Tabelul 1.
Tabel în dimensiune completă
Caracteristicile transplantului
Tabel în dimensiune completă
Curs post-transplant
Tabelul 3 rezumă rezultatele post-transplant ale cohortei noastre. Un pacient a murit în ziua +10 (eveniment septic) și într-o zi +14 (progresia bolii). Din cei 42 de pacienți evaluabili, 39 au obținut aderența (93%). Timpul mediu până la greutatea neutrofilelor a fost de 15 zile (interval 10-42). Doi pacienți au avut o recidivă la grefă (5%). GvHD acut a fost raportat la 23 de pacienți (52%) și a fost sever la opt pacienți (19%). Un pacient a avut GvHD cronică limitată și două extinse, incidența generală a fost de 7%. GvHD a fost considerat a fi cauza decesului la doi pacienți din grupul nostru.
Tabel în dimensiune completă
Rezultatul
Nouă pacienți au murit în Republica Cehă din cauze legate de transplant (două legate de GVHD, o toxicitate cardiacă, o infecție cu Aspergillus toracic, o encefalită, o infecție legată de CMV, o sepsis, o endocardită, o pneumonie legată de adenovirus). Cinci dintre acești opt pacienți au murit înainte de ziua +100 după SCT. TRM în ziua +100 și ziua +365 a fost de 11% (IÎ 95% 4-23%) și 18% (IÎ 95% 9-31%).
Dintre cei 44 de pacienți, 30 (68%) au obținut RC după SCT. Optsprezece persoane locuiesc în Republica Cehă și 5 ani LFS în acest grup a fost de 43% (IC 95% 28-57%), cu o urmărire mediană de 6 ani și 9 luni. Saptesprezece pacienti au recidivat la un timp mediu de 61 de zile dupa SCT (interval 13 - 279) si toti au murit de progresia bolii. Un pacient care a recidivat a intrat într-un alt CR după un tratament ulterior care a suferit un al doilea SCT, după care a recidivat și a murit din cauza progresiei bolii. Incidența cumulativă a recăderii a fost de 32% după 5 ani (IÎ 95% 19-46%).
Analiza subgrupului
Riscul de recurență și mortalitate non-recidivantă a fost similar la pacienții cu boală refractară primară și refractară recurentă (Figura 1). Ca rezultat, LFS și OS pe 5 ani la pacienții cu LMA refractară primară (43% (IÎ 22-62%) și 43% (IÎ 22-62%)) s-au suprapus cu pacienții cu boală refractară recidivantă (43% (IÎ 22 -62%)). –62%) și 43% (CI 22-62%)) (Figura 2). În mod similar, pacienții cu citogenetică adversă nu au avut rezultate mai slabe decât pacienții cu citogenetică standard (rata de recădere cumulativă 29% față de 42%, P = 0,345). În schimb, niciunul dintre pacienții cu un profil citogenetic favorabil nu a recidivat după transplant (Figura 3) și LFS pe 5 ani a fost de 67% (CI 19-90%), deși acest lucru nu a atins semnificația statistică din cauza numărului scăzut de pacienți în acest caz. (n = 6).
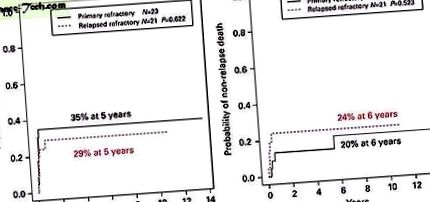
A ) Incidența cumulativă a recidivelor după SCT la copiii cu LMA refractară primară și copiii cu LMA refractară recidivată. ( b ) Incidența cumulativă a mortalității fără recidivă după SCT la copiii cu LMA refractară primară și copiii cu LMA refractară recidivată. Versiunea color a acestei imagini este disponibilă în Transplantul de măduvă osoasă online.
Imagine la dimensiune completă
A ) Supraviețuire fără leucemie după SCT la copii cu LMA refractară primară și copii cu LMA refractară recidivată. ( b ) Supraviețuirea globală după SCT pentru copiii cu LMA refractară primară și copiii cu LMA refractară recidivată. Versiunea color a acestei imagini este disponibilă în Transplantul de măduvă osoasă online.
Imagine la dimensiune completă
Incidența cumulativă a recidivelor după SCT la copiii cu LMA refractară în funcție de grupul de risc citogenetic la diagnostic. Grupuri de risc citogenetic conform Swerdlow și colab. 16 și Creutzig și colab. 6 O versiune color a acestei imagini este disponibilă în Transplantul de măduvă osoasă online.
Imagine la dimensiune completă
Tabelul 4 rezumă factorii de prognostic analizați pentru LFS, incidența recidivelor și rata de recurență a mortalității în grupul nostru. Analiza de regresie a arătat că transplantul cu un procent de explozii mai mare de 30% în BM a prezis un risc semnificativ mai mare de recidivă (60% vs. 15%, P = 0,004), în timp ce aportul mieloablativ și dezvoltarea GVHD acut au afectat pozitiv rezultatul grup de pacienți. (Figura 4a). Nicio altă caracteristică legată de transplant (donator, sursă de celule stem, epuizare a celulelor T) nu a afectat rezultatul pe termen lung. Pacienții cu vârsta 10 ani au arătat o tendință spre creșterea mortalității legate de transplant (5% față de 29%, P = 0,05).
Tabel în dimensiune completă
A ) Supraviețuirea fără leucemie la copiii care primesc stabilizare mieloablativă (MAC) și care dezvoltă GVHD acut comparativ cu copiii care nu dezvoltă GVHD acut și care au o intensitate de condiționare redusă (RIC). b ) Supraviețuirea fără leucemie la copiii cu vârsta de 10 ani care au suferit SCT cu> 30% explozii în măduva osoasă comparativ cu toți ceilalți pacienți din grup. Versiunea color a acestei imagini este disponibilă în Transplantul de măduvă osoasă online.
Imagine la dimensiune completă
Prin combinarea factorilor de risc de mai sus, am reușit să identificăm un grup de copii cu un risc foarte mare de recidivă. Pacienții cu vârsta de 10 ani cu> 30% explozii în SCT au avut rezultate semnificativ mai slabe decât restul populației noastre, ceea ce sa dovedit a fi aproape nedetectabil (LFS 10% față de 53%, P = 0,037, Figura 4b).
discuţie
Deși SCT este adesea utilizat pentru a trata LMA cu risc crescut, rolul său în contextul bolilor chimioterapeutice este încă dezbătut. Acest studiu a examinat rolul SCT la pacienții copii și adolescenți cu LMA refractară și caracteristici prognostice în acest sens. Seria noastră arată că SCT poate fi tratat la un număr semnificativ de copii transplantați cu LMA activă, cu un VZPS de 5 ani de 43%. În special, am arătat că pacienții mai tineri cu o sarcină scăzută a bolii în SCT au atins o LFS remarcabilă de 53%. Una dintre principalele limitări ale studiului nostru este că natura registrului exclude o evaluare a numărului de cazuri de LMA refractară care au fost diagnosticate în timpul perioadei de studiu în Regatul Unit, omițând informații importante cu privire la numărul de pacienți care au fost considerați inadecvati pentru SCT sau au decedat. în timpul tratamentului. în așteptarea SCT (estimăm că aproximativ 120 de pacienți cu LMA refractară au fost diagnosticați în Regatul Unit în perioada de studiu). La rândul său, aceasta duce la o tendință semnificativă de selecție în cohorta noastră de pacienți.
În plus, 18 pacienți din grupul nostru au fost diagnosticați cu boală refractară pe SCT pe baza evaluării morfologice a BM singur fără confirmare moleculară sau citogenetică. În timp ce evaluarea morfologică implică un anumit grad de subiectivitate, în acest studiu, incidența recidivelor la pacienții diagnosticați cu tratament refractar bazat exclusiv pe morfologie nu a fost statistic diferită de incidența pacienților cu confirmare moleculară/citogenetică (incidența recidivelor 53% vs. 30 %). P = 0, 1, CI 0, 8 - 6, 5).
În limitele studiului de registru retrospectiv, datele noastre indică faptul că o proporție semnificativă de copii cu LMA refractară activă pot fi tratați cu SCT, în special cei cu citogenetică favorabilă, pacienți cu vârsta sub 10 ani și mai puțin de 30% din explozii în BM la copii. SCT. Acest studiu sugerează, de asemenea, că un regim de condiționare mieloablativă, precum și strategii de îmbunătățire a GVL pot fi benefice în acest context. Conform datelor noastre, transplantul nu pare să ofere o șansă semnificativă de vindecare a pacienților cu vârsta peste 10 ani și explozii> 30% în BM. Prin urmare, acest grup de copii ar trebui evaluat cu atenție pe baza fazei 1/tratament nou sau a studiilor de îngrijire paliativă în funcție de starea lor clinică și de înclinația familială.