- obiecte
- abstract
- introducere
- Degenerescența maculară legată de vârstă
- Β - extensie, structură și asamblare dinamică
- Mecanisme de acțiune Aβ în neuronii degenerativi
- Dovezi ale Aβ la nivelul retinei în vârstă și al DMA
- Formarea Aβ constitutivă în retina normală
- Diafragma retiniană a retinei crește odată cu înaintarea în vârstă
- Agregare p este implicat în etapele cheie ale AMD
- P- depozitele retiniene declanșează microambiente pro-inflamatorii și proangiogene
- Factorii de risc AMD promovează A β agregare în retina îmbătrânită
- Modele animale de AMD și tratament anticorp anti-Aβ
- Β și AMD - lecții despre neurodegenerare și acțiuni ulterioare
obiecte
abstract
Degenerescența maculară legată de vârstă (DMA) este o tulburare oculară complexă care afectează o zonă critică a retinei cunoscută sub numele de macula, care este critică pentru vederea centrală și percepția detaliilor fine. Boala este principala cauză a orbirii ireversibile în societățile ale căror date demografice favorizează creșterea vârstei. Etiologia acestei tulburări degenerative este puțin cunoscută, dar include atât factori de risc genetici, cât și de mediu. 1, 2, 3 esențială pentru patologia degenerativă este pierderea funcției vizuale care este asociată cu atrofia fotoreceptorului și epiteliul pigmentar retinian subiacent (RPE), care formează bariera hemato-retiniană. 4, 5 Celulele ganglionare ale retinei (RGC) și monostratul RPE au fost identificate recent ca o sursă majoră de sinteză și secreție beta amiloid (Aβ) în ochiul posterior. 6 Aβ este o proteină extrem de penetrantă și foarte toxică, care vizează agresiv neuronii și este o caracteristică cheie a bolii neurodegenerative. 7, 8 Au fost descoperite mai multe rezervoare Aβ în ochi în mediul retinian, în timp ce niveluri ridicate de Aβ au fost găsite în retina îmbătrânită și asociate cu etapele cheie ale progresiei AMD. 6 Aceste descoperiri susțin ipoteza că Aβ joacă un rol crucial, deși anterior necaracterizat, în conducerea proceselor degenerative în macula îmbătrânită.
Aici adunăm cele mai recente cunoștințe din literatura de specialitate care examinează DMA, neurodegenerarea, precum și biologia β-structurală, care susțin ipoteza noastră și oferă informații despre evenimentele degenerative de bază care ar putea agrava retina îmbătrânită. O mai bună înțelegere a modului în care Aβ ar putea viza funcția retiniană poate ajuta la proiectarea de noi terapii pentru tratamentul DMAV în viitor.
Degenerescența maculară legată de vârstă
DMI este cea mai frecventă cauză a orbirii ireversibile în societățile care îmbătrânesc și afectează la nivel global
50 de milioane de persoane cu un cost direct estimat la aproape 255 miliarde de dolari. 9 Boala afectează
Deși AMD a fost caracterizată clinic, mecanismele de bază, în special în timpul bolii timpurii, rămân incomplet cunoscute. Lipsa de caracterizare moleculară între AMD uscată și umedă ne-a limitat, așadar, înțelegerea și definiția bolii la observații și terminologie clinice predominante. Descoperirea recentă a Ap în retina îmbătrânită și asocierea acesteia cu AMD reprezintă o oportunitate interesantă de a privi AMD dintr-o nouă perspectivă și de a înțelege mai bine debutul și progresia bolii cu noi termeni moleculari.
Β - extensie, structură și asamblare dinamică
Gena proteinei precursoare amiloid (APP) localizată pe cromozomul 21q21 codifică glicoproteina membranară integrală de tip I exprimată omniprezent în mai multe forme alternative de îmbinare, dintre care cele mai frecvente izoforme includ APP 751, APP 770 și APP 695. Transcrierile și proteinele APP sunt raportate a fi exprimate abundent în celulele RGC și RPE umane murine, de șobolan, precum și umane, 14, 15, iar APP 695 este izoforma majoră exprimată în creier. 16 Funcția (funcțiile) APP rămân incomplete, majoritatea studiilor sugerând semnalizarea prin mai multe căi din creier. 17 Prelucrarea proteolitică a APP are loc prin două căi care se exclud reciproc, denumite căi amiloidogene și neamiloidogene (sau constitutive). 18, 19 Scindarea treptată a APP pe calea amiloidogenă de către enzimele β- și γ-secretază produce o peptidă monomerică Aβ cu greutate moleculară
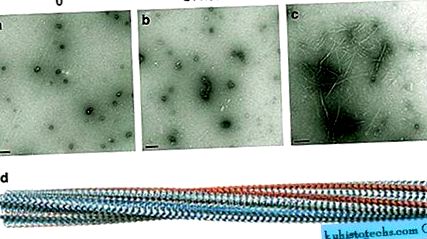
(a - c) Vedeți micrografiile cu electroni negativi colorate care arată auto-asamblarea Aβ 1-42 la pH 7,4, 50 μM. (a) Prezintă oligomeri sferici mici, care sunt vizibili imediat după prepararea peptidei Aβ 1-42. (Soura și colab. 50). Sunt asamblate în continuare în 24 de ore pentru a forma (b) protofibrile alungite și în cele din urmă (c) fibrile amiloide după 48 de ore de incubație. d Prezintă un model structural de fibră amiloidă compusă din structura ß și care prezintă o arhitectură răsucită lent. Generarea modelului este descrisă în Morris și colab. 101
Imagine la dimensiune completă
Mecanisme de acțiune Aβ în neuronii degenerativi
Dovezi ale Aβ în retina îmbătrânită și AMD
Formarea Aβ constitutivă în retina normală
Atât retina, cât și sistemul nervos central (SNC) au o origine comună, deoarece ambele sunt derivate din tubul neural în curs de dezvoltare. Ambele structuri sunt strâns legate de vasculatura adiacentă de-a lungul barierelor hemato-retiniene și hematoencefalice. Odată cu înaintarea în vârstă, atât retina, cât și creierul dezvoltă depozite extracelulare asociate cu patologia degenerativă, denumite plăci drusene și senile. Prin urmare, nu este surprinzător faptul că multe asemănări izbitoare între plăcile drusen și senile includ Aβ. Alte componente partajate includ următoarele; component al amiloidului seric P, apolipoproteinei E, imunoglobulinei, matricei membranei bazale, proteoglicanilor și ionilor metalici (Fe 3+, Cu 2+ și Zn 2+), reactanți de fază acută, elemente legate de protează/clearance și mai multe proteine complementare ca și alți mediatori inflamatori care sugerează inflamația locală asociată în mod tipic cu depozitele retiniene. Astfel de asemănări remarcabile între plăcile drusen și senile, care sunt în concordanță cu vârsta și prognosticul clinic slab, sugerează că mecanisme patologice similare pot duce la modificări degenerative atât în retină, cât și în creier.
Diafragma retiniană a retinei crește odată cu înaintarea în vârstă
Depunerea Ss cu vârsta în creștere nu s-a limitat la regiunile sub-RPE, dar s-a constatat că se acumulează în mod neașteptat în segmentele exterioare ale fotoreceptorului (POS) la șoareci mai în vârstă. Astfel de depozite au fost identificate după doar 3 luni, iar la 12 luni segmentele exterioare au fost complet înfășurate în material care conțin Aβ, care părea să fie diferit calitativ în termen de 24 de luni. 60 Deși nu există dovezi directe că un astfel de material este pur Aβ, legătura strânsă dintre modelele Aβ imunocolorate și scanarea imaginilor EM afirmă că Aβ este cel puțin un element al unor astfel de depozite legate de vârstă. În plus, injecția intravitreală de Aβ40 oligomerică la șobolani de tip sălbatic a produs cele mai ridicate niveluri de intensitate a imunocolorării în POS, susținând ideea acumulării preferențiale de Aβ în proximitatea apicală a celulelor RPE. Analiza probelor umane post-mortem cu vârsta cuprinsă între 31 și 90 de ani a reflectat un model similar de creștere a imunocolorării Aβ în POS. 60 Acest model de acumulare de Aβ, care începe de la vârful apical al POS și continuă în lungime, ilustrează agregarea specifică a Aβ, 60 și ca atare este de acord cu alte descoperiri 14, 54, 55, 56, care prezintă Aβ retiniană/Acumularea RPE. în ochiul posterior cu înaintarea în vârstă (Figura 2).
Schema care prezintă mai multe situri de sinteză, secreție și agregare de Aβ în retina îmbătrânită (asterisc roșu), care este raportată în literatura de specialitate. BrM, membrana lui Bruch; POS, segmente exterioare ale fotoreceptorului; RGC, celule ganglionare ale retinei; RPE, epiteliu pigmentar retinian.
Imagine la dimensiune completă
Agregarea p este implicată în etapele cheie ale AMD
Grupurile Aβ sunt predominante la indivizii cu niveluri de drusen moderate până la ridicate. Aβ este aranjat în structuri sferice numite "vezicule amiloide", care pot ocupa o mare parte din volumul drusen și pot crea site-uri potențiale de activare a complementului. Drusenul poate fi dens ambalat în mai multe vezicule amiloide sau poate conține o singură veziculă mare. Prezența diferitelor structuri Aβ poate reflecta natura evoluției dronelor cu progresie a bolii. De exemplu, prezența mai multor nuclee oligomerice într-un drusen mare se poate datora unei mai mici aglomerări a drunturilor în timp. Ap în drusen se corelează cu fotoreceptorii degeneratori și RPE. CC, choriocapillaris; BrM, membrana lui Bruch; RPE, epiteliu pigmentar retinian.
Imagine la dimensiune completă
Depozitele P din retină declanșează microambiente pro-inflamatorii și proangiogene
Factorii de risc AMD promovează agregarea β în retina îmbătrânită
Modele animale de AMD și tratament anticorp anti-Aβ
Ca boală degenerativă legată de vârstă, cu o etiologie complexă, reproducerea întregului spectru al patologiei AMD în modele animale. Cu toate acestea, acest lucru nu a împiedicat dezvoltarea multor modele animale de rozătoare, iepuri, porci și primate neumane. Modelele de șoareci/șobolani utilizate pe scară largă au avantajul unui cost mai mic, ușurința întreținerii și capacitatea de a dezvolta simptome ale bolii într-o perioadă relativ scurtă de timp, dar suferă de defecte, dintre care majoritatea includ orbirea este deficiența maculară. În mod critic, niciun model unic nu a avut succes în reproducerea întregului spectru al bolilor AMD, deși există modele convingătoare care reproduc caracteristici limitate ale formelor geografice și exudative ale bolii. În schimb, utilizarea primatelor non-umane oferă posibilitatea de a studia DMA într-un sistem care are o asemănare și fiziologie mai strânse cu oamenii, dar are mai multe dezavantaje, inclusiv implicații etice semnificative, probleme de manipulare genetică și scale de timp mai lungi. până la debutul bolii.
Β și AMD - lecții din neurodegenerare și pași suplimentari
Aici, am discutat ipoteza și noile descoperiri interesante care arată că Aβ are capacitatea de a juca un rol cheie în AMD, al cărui studiu poate oferi o mai bună înțelegere a mecanismelor bolii timpurii, precum și a căilor moleculare care mențin retina cronică. degenerare. Exemplele de patologie comună la pacienții cu AD includ grosimea redusă a stratului de fibre nervoase, 99 circulația sanguină anormală a retinei, 62, precum și grosimea redusă a coroidei, 100 de locuri în care degenerarea apare și în glaucom și AMD. 1, 5, 74 Trăsături similare se găsesc și între plăcile senile AD și drusen AMD6, precum și un model de afectare selectivă a țesuturilor, sugerând mecanisme moleculare comune cel puțin în unele etape ale acestor boli. Studiile despre Aβ și patologia retiniană conexă au potențialul de a oferi noi perspective asupra DMA și de a aborda această boală orbitoare debilitantă dintr-o nouă perspectivă. Astfel de investigații sunt deja în desfășurare în laboratorul nostru.
- Mașină albastră BETA GLUCAN 500ML
- Vrei ca copiii să renunțe la fumat; Infertilitate; Când nu funcționează
- Supa de broccoli - crema, Dieta divizata - retete, reteta
- Ziua D în calitate de decoratoare Aneta și echipa ei de la agenția de nunți La Bella Idea aparțin pentru a vă economisi timpul,
- Ziua D cu un an după și cu o săptămână înainte